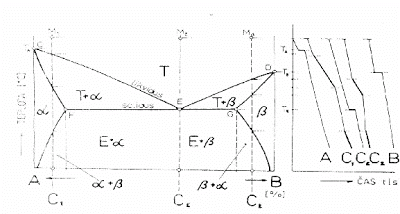
6. Rovnovážný diagram dvou složek omezeně rozpustných v tuhém stavu, popis chladnutí slitiny
 • jde o velmi častý případ krystalizace binárních slitin, – prakticky u všech dvojic kovů nalézáme alespoň určitou rozpustnost za vyšší teploty
• jde o velmi častý případ krystalizace binárních slitin, – prakticky u všech dvojic kovů nalézáme alespoň určitou rozpustnost za vyšší teploty
• z diagramu plyne že kovy A a B jsou dokonale rozpustné v kapalném stavu, – krystalizace jednotlivých slitin počíná za teploty která odpovídá dvěma křivkám likvidu L1 a L2 které se protínají opět v eutektickém bodě, – na eutektickou přímku FEG navazují na obou stranách křivky solidu CF a GD, – tyto křivky určují oblast vzájemné rozpustnosti, – eutektická přímka pak určuje oblast vzájemné nerozpustnosti
• v rozsahu koncentrací A až H vzniká primární krystalizací tuhý roztok a, – v rozsahu koncentrací J až B tuhý roztok b, – oba tuhé roztoky tvoří koncové fáze diagramu, – rozpustnost je však u obou roztoku rozdílná, – zatímco segregační čára G až J vyjadřuje konstantní rozpustnost, – segregační čára F až H rozpustnost závislou na teplotě, – druhý případ je mnohem více častější
• střední část rovnovážného diagramu H až J je tvořena eutektickou směsí obou tuhých roztoků (a+b), – ve slitinách o koncentraci H až É se nachází primárně vyloučený tuhý roztok a v eutektiku, – ve slitinách o koncentraci É až J je v eutektiku uložen primárně krystalizující tuhý roztok b